- Anúncios -
O que significa listo em Espanhol?
O que significa "listo" em espanhol? Essa palavra tem um significado interessante e versátil. Pode significar "pronto", como em "Estou listo para sair". Mas também pode ser usado para descrever alguém esperto ou inteligente. É um termo que demonstra habilidade e preparo em diversas situações. Agora que você sabe o significado, está listo para usá-lo corretamente!
O que significa grant?
O que significa "grant"? Essa palavra, que vem do inglês, pode ter diferentes significados em português. Pode se referir a uma concessão de dinheiro, um subsídio ou até mesmo uma autorização ou permissão concedida. O termo é versátil e possui amplas aplicações em diferentes contextos. Vamos explorar mais sobre essa interessante palavra e suas nuances.
O que significa stranger?
Misterioso, intrigante, enigmático. Quando nos deparamos com alguém desconhecido, surge a pergunta: O que significa Stranger? Mais do que simplesmente um estranho, essa palavra carrega consigo tanto mistério quanto possibilidades. Exploraremos a essência desse termo e revelaremos como um encontro inesperado pode transformar nossas vidas de maneiras surpreendentes.
Medicina
O quê significar ser hipervitamínico?
Ser hipervitamínico significa exceder a quantidade segura de vitaminas no organismo. Embora…

Create an Amazing Newspaper
Siga-nos
O que significa antilogaritmo na matemática?
Antilogaritmo, uma palavra intrigante no mundo da matemática. Mas o que será…
O que significa hipotenusa?
A hipotenusa é como aquele amigo que sempre dá o suporte necessário,…
O que significa expressão numérica?
A expressão numérica, um enigma matemático envolto em símbolos, números e operações.…
O que significa escalar na matemática?
Você já se perguntou o que significa escalar na matemática? Bem, imagine-se…
O que significa multiplicação?
A multiplicação é como uma poção mágica matemática que transforma um número…
O que significa equação diferencial na matemática?
Resolver equações diferenciais pode ser desafiador para muitos estudantes de matemática, mas…
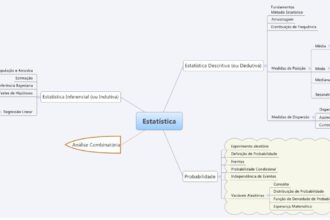
O que significa estatística na matemática?
A estatística na matemática é como uma lente que nos permite enxergar…
O que significa aproximação na matemática?
A aproximação na matemática é uma poderosa ferramenta que nos permite obter…

Create an Amazing Newspaper
Conteúdo patrocinado
O que significa capitalismo?
O que significa capitalismo? É um conceito que se desdobra em um verdadeiro oceano de interpretações e debates. Desde sua origem na Revolução Industrial até os dias atuais, o capitalismo abrange os pilares da propriedade privada, da livre iniciativa e do mercado competitivo. Mas, será que esse sistema econômico tem se mostrado eficiente e sustentável para todos? Exploraremos essas questões e muito mais neste artigo, mergulhando nas profundezas desse complexo sistema que molda nossa sociedade contemporânea.
O que significa IPVA?
Você já se perguntou o que significa IPVA? Essa sigla misteriosa tem gerado dúvidas e até dores de cabeça para muitos brasileiros. Mas não se preocupe, aqui vamos desvendar o…
Top Autores
Stay Up to Date
Subscribe to our newsletter to get our newest articles instantly!