- Anúncios -
O que significa unlike?
O que significa "unlike"? Essa é uma pergunta que muitas vezes nos fazemos ao navegar pelas redes sociais. Esse pequeno botão, com a tímida aparência de um dedo indicador apontado para baixo, desperta curiosidade e incita o questionamento sobre o seu real significado. Seria uma forma de desaprovação? Ou apenas uma maneira de indicar que algo não nos agrada? Descubra…
O que significa finding?
Encontrar, resgatar, desvendar... A palavra "finding" tem um encanto misterioso, que envolve descobertas e revelações. Mas, afinal, o que significa "finding"? Neste artigo, mergulhamos no significado dessa palavrinha e exploramos suas nuances. Se prepare para se surpreender com o que está por trás do encontrar.
O que significa ban?
O ban, abreviação de "banimento", é um termo popularmente utilizado em comunidades online para descrever a ação de excluir ou restringir o acesso de um usuário. Descubra o significado por trás dessa palavra e desvende os mistérios do banimento virtual.
Medicina
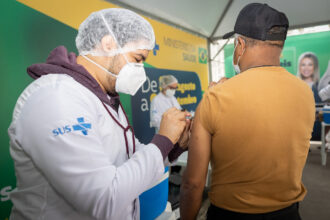
O que significa câncer de cólon ou reto?
O câncer de cólon ou reto é uma doença que assombra milhões…

Create an Amazing Newspaper
Siga-nos
O que significa equações polinomiais?
Você já se perguntou sobre o significado das equações polinomiais e como…
O que significa associação na matemática?
Já se questionou sobre o que significa associação na matemática? Muito além…
O que significa aceleração na matemática?
A aceleração, na matemática, é um conceito fundamental que nos permite entender…
O que significa equações racionais?
Você já se perguntou o que significa equações racionais? Bem, essas equações…
O que significa teorema?
O teorema, um termo comumente usado na matemática, é como uma joia…
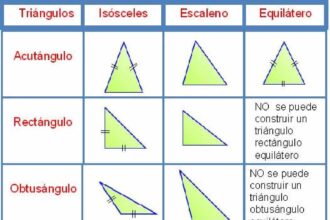
O que significa escaleno?
Escaleno, uma palavra que encerra mistério e equilíbrio. Entre os triângulos, este…
O que significa expressão numérica?
A expressão numérica, um enigma matemático envolto em símbolos, números e operações.…
O que significa dividendo?
Você já se perguntou o que significa dividendo? Essa é uma palavrinha…

Create an Amazing Newspaper
Conteúdo patrocinado
O que significa capitalismo?
O que significa capitalismo? É um conceito que se desdobra em um verdadeiro oceano de interpretações e debates. Desde sua origem na Revolução Industrial até os dias atuais, o capitalismo abrange os pilares da propriedade privada, da livre iniciativa e do mercado competitivo. Mas, será que esse sistema econômico tem se mostrado eficiente e sustentável para todos? Exploraremos essas questões e muito mais neste artigo, mergulhando nas profundezas desse complexo sistema que molda nossa sociedade contemporânea.
O que significa CNAE?
Você já ouviu falar em CNAE? É a sigla para Classificação Nacional de Atividades Econômicas, um código que identifica a atividade principal de uma empresa. Quer entender mais sobre o…
Top Autores
Stay Up to Date
Subscribe to our newsletter to get our newest articles instantly!