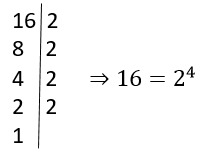- Anúncios -
O que significa platform?
Você já se perguntou o que significa platform? Essa palavra, de origem inglesa, pode ter vários significados, dependendo do contexto. Pode se referir a uma plataforma digital, uma estrutura elevada ou até mesmo a uma base de lançamento. Descubra mais sobre esse termo versátil e multifacetado neste artigo.
O que significa ring?
Um anel é mais do que um simples objeto de adorno. Ele carrega consigo um significado especial, representando compromisso, união e amor. Descubra neste artigo o verdadeiro significado por trás do icônico anel e suas diferentes simbologias.
O que significa Diciembre em Espanhol?
O mês de dezembro é rico em significados e tradições em várias culturas ao redor do mundo, inclusive na Espanha. Mas afinal, o que significa Diciembre em espanhol? Este termo, derivado do latim "decem", que significa dez, representa o último mês do ano, carregado de festividades, celebrações e reflexões sobre o ano que se encerra. Com suas festas tradicionais como…
Medicina
O quê significar ser hiperproteico?
Você já ouviu falar sobre alimentação hiperproteica e ficou curioso(a) para saber…

Create an Amazing Newspaper
Siga-nos
O que significa algoritmo?
Você já ouviu falar em algoritmo, mas sabe o que isso realmente…
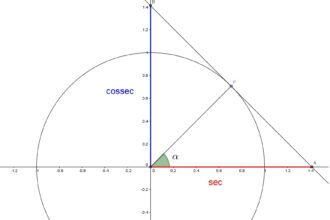
O que significa trigonometria na matemática?
O que é a trigonometria? Para alguns, é o estudo dos números…
O que significa radiciação?
A radiciação é como um delicado desvendar, um mergulho profundo em busca…
O que significa acumulação na matemática?
A acumulação é um conceito matemático fascinante que nos permite entender o…
O que significa algoritmo na matemática?
Algoritmo na matemática é como uma incrível coreografia numérica, uma dança entre…
O que significa cosseno na matemática?
O cosseno é uma das grandezas fundamentais da matemática, mas seu significado…
O que significa teorema?
O teorema, um termo comumente usado na matemática, é como uma joia…
O que significa aceleração na matemática?
A aceleração, na matemática, é um conceito fundamental que nos permite entender…

Create an Amazing Newspaper
Conteúdo patrocinado
O que significa capitalismo?
O que significa capitalismo? É um conceito que se desdobra em um verdadeiro oceano de interpretações e debates. Desde sua origem na Revolução Industrial até os dias atuais, o capitalismo abrange os pilares da propriedade privada, da livre iniciativa e do mercado competitivo. Mas, será que esse sistema econômico tem se mostrado eficiente e sustentável para todos? Exploraremos essas questões e muito mais neste artigo, mergulhando nas profundezas desse complexo sistema que molda nossa sociedade contemporânea.
O que significa TL;DR?
Você já se deparou com a sigla TL;DR em textos online e ficou se perguntando o que diabos isso significa? TL;DR, ou "Too Long; Didn't Read", é uma expressão utilizada…
Top Autores
Stay Up to Date
Subscribe to our newsletter to get our newest articles instantly!