- Anúncios -
O que significa motor?
O motor é a essência da energia em movimento, uma força silenciosa que impulsiona e dá vida às máquinas. É a sinergia entre engenharia e mecânica, transformando combustível em poder. O motor é o coração pulsante das inovações tecnológicas, uma ODALISCA moderna que dança aos comandos do progresso. No fundo, o motor é a própria definição da evolução, do poder…
O que significa childhood?
A infância pode ser um mistério envolto em nostalgia e inocência. Para entender o que significa infância, é preciso mergulhar em memórias cheias de brincadeiras, descobertas e sonhos. É um tempo mágico, onde a imaginação floresce sem limites, e onde a pureza e a alegria são componentes essenciais. É uma fase transitória repleta de aprendizados e laços afetivos que moldam…
O que significa democratic?
O que realmente significa "democrático"? O termo evoca no nosso imaginário um sistema em que o povo possui o poder de tomar decisões coletivas. Mas será que essa definição é suficiente para capturar toda a complexidade desse conceito? Ser "democrático" vai além da simples participação popular e engloba a garantia dos direitos fundamentais, a igualdade, a inclusão e o respeito…
Medicina
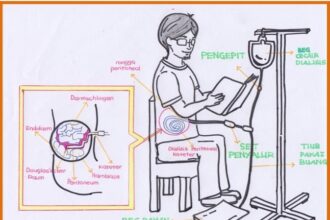
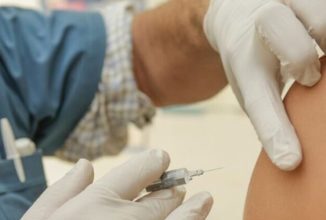
O que significa insuficiência renal crônica?
A insuficiência renal crônica é um termo que carrega em si um…

Create an Amazing Newspaper
Siga-nos
O que significa escalar na matemática?
Você já se perguntou o que significa escalar na matemática? Bem, imagine-se…
O que significa adição na matemática?
Quando mergulhamos no mundo da matemática, nos deparamos com diferentes termos e…
O que significa derivada na matemática?
Derivada na matemática é como uma chave mágica que nos permite desvendar…
O que significa radiciação?
A radiciação é como um delicado desvendar, um mergulho profundo em busca…
O que significa álgebra?
Um mundo de incógnitas e equações complexas, álgebra é um ramo fascinante…
O que significa equações exponenciais?
Você já se perguntou o que significam equações exponenciais? Essas equações misteriosas,…
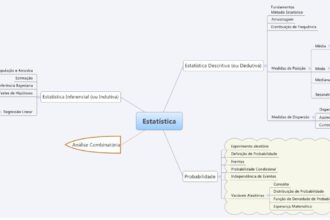
O que significa estatística na matemática?
A estatística na matemática é como uma lente que nos permite enxergar…
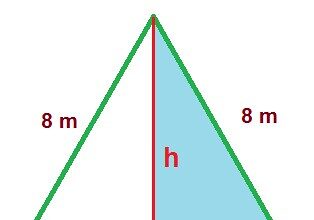
O que significa equilátero?
No mundo da geometria, a palavra "equilátero" evoca harmonia, perfeição e equidade.…

Create an Amazing Newspaper
Conteúdo patrocinado
O que significa capitalismo?
O que significa capitalismo? É um conceito que se desdobra em um verdadeiro oceano de interpretações e debates. Desde sua origem na Revolução Industrial até os dias atuais, o capitalismo abrange os pilares da propriedade privada, da livre iniciativa e do mercado competitivo. Mas, será que esse sistema econômico tem se mostrado eficiente e sustentável para todos? Exploraremos essas questões e muito mais neste artigo, mergulhando nas profundezas desse complexo sistema que molda nossa sociedade contemporânea.
O que significa IRPF?
O que significa IRPF? Essa sigla faz referência ao Imposto de Renda Pessoa Física, uma obrigação tributária anual para os cidadãos brasileiros. Neste artigo, exploraremos de forma criativa e neutra…
Top Autores
Stay Up to Date
Subscribe to our newsletter to get our newest articles instantly!